Autor/a: Glenn T. Furuta y David A. Katzka Fuente: N Engl J Med 2015;373:1640-8 Eosinophilic Esophagitis
Introducción:
Antes considerada una enfermedad rara, la esofagitis eosinofílica (EE) es ahora una de las condiciones más comunes diagnosticadas durante la evaluación de los problemas de alimentación en los niños y en los adultos con disfagia e impactación de alimentos. La entidad existe en todo el mundo pero ha sido más ampliamente estudiada en los países occidentales, donde se estima que su prevalencia es del 0,4% de la población infantil y adulta. No hay certeza si la EE es realmente una enfermedad nueva o simplemente una enfermedad que solo ha sido reconocida recientemente.
Definición y diagnóstico diferencial
Inicialmente, la EE era considerada únicamente como una manifestación de la enfermedad por reflujo gastroesofágico (ERGE). Sin embargo, a mediados de la década de 1990, los especialistas identificaron a la EE en los adultos y los niños que tenían otros síntomas.
En estos pacientes, ni los síntomas clínicos ni los cambios histológicos respondían a la supresión del ácido o a la cirugía antirreflujo, lo que sugirió que la condición era distinta de la ERGE. Dos estudios de series de casos y la evidencia de que la EE se resuelve en respuesta a la terapia con una dieta de fórmula elemental sugirieron que la EE es una entidad única. Sin embargo, había muy pocos criterios diagnósticos claros.
Más recientemente, se han desarrollado recomendaciones para su evaluación y tratamiento, basadas en las experiencias clínicas de diferentes subespecialidades médicas y en el mayor conocimiento derivado de las investigaciones básicas y clínicas.
Actualmente, la EE se define como una enfermedad crónica mediada por la inmunidad o por antígenos, que se caracteriza por síntomas relacionados con la disfunción esofágica y la inflamación predominantemente eosinofílica. Los antígenos dominantes que median en esta enfermedad parecen estar en los alimentos.
Clínicamente, la EE está definida por varios componentes.
Primero: los síntomas incluyen problemas alimentarios (aunque no se limitan a ellos), vómitos y dolor abdominal en los niños y, disfagia e impactación de alimentos en los adolescentes y adultos.
Segundo: la eosinofilia de la mucosa esofágica es de al menos 15 eosinófilos por campo de gran aumento. Antes estos hallazgos, se deben descartar otras causas, particularmente la ERGE. Sin embargo, esta enfermedad puede ser difícil de descartar, porque ni la respuesta a los inhibidores de la bomba de protones (IBP) ni la duración de la exposición del esófago al ácido, medida por el monitoreo ambulatorio del pH, distinguen definitivamente a la ERGE de la EE. Otras causas raras de EE son la infección parasitaria, la vasculitis alérgica, la leiomiomatosis esofágica y la enfermedad de Crohn del esófago.
Patogénesis
Predisposición a la esofagitis eosinofílica por factores ambientales
La creciente prevalencia de la EE ha centrado la atención en las exposiciones ambientales. El nacimiento por cesárea, el parto prematuro, la exposición a los antibióticos durante la infancia, la alergia alimentaria, la falta de lactancia materna y la residencia en una zona de menor densidad de población han sido asociados a la EE, lo que puede significar que la alteración de la estimulación del sistema inmunológico a una edad temprana confiere una predisposición a esa enfermedad.
Los estudios también han sugerido que la falta de exposición temprana a los microbios y la presencia de un microbioma alterado pueden influir en su desarrollo, como se ha sugerido para otras enfermedades atópicas, como el asma y la dermatitis atópica. Se especula que estas exposiciones tempranas en la vida crean una firma epigenética que aumenta la probabilidad de desarrollar EE.
Predisposición genética
El predominio masculino de la EE así como los estudios de la historia familiar y doble concordancia, y los estudios de asociación genómica indican que en la EE hay un componente genético. En casi todos los estudios, el sexo masculino tiene una preponderancia de 3:1.
Con frecuencia, se halla una historia familiar de EE, con un riesgo de herencia estimado en el 2% sobre la base de los resultados de una cohorte de familia nuclear de 914 probandos con EE y 63 probandos gemelos. Los estudios de asociación de todo el genoma han informado 3 genes con secuelas funcionales propuestas (genes que codifican la linfopoyetina del estroma tímico, la eotaxina-3, también denominada ligando motivo 26 de la quimiocina CC y, la calpaína-4) por estar alterados en la EE.
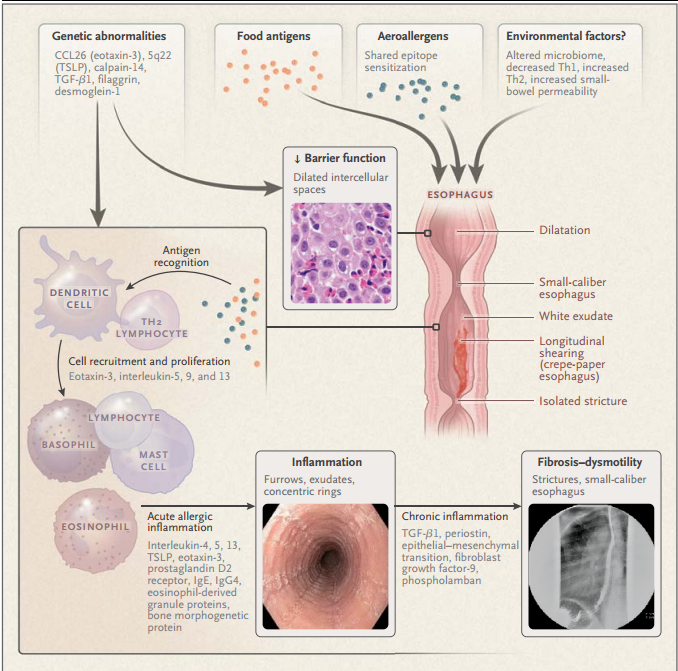
Deterioro de la función de barrera
La evaluación de los tejidos del esófago de los pacientes con EE revela un sorprendente patrón de espacios interepiteliales dilatados, alteración de la barrera epitelial y baja regulación de las proteínas asociadas a la función de barrera (filagrina y zonulina-1) y moléculas de adhesión (desmogleína-1).
In vitro, se ha demostrado que la interleucina-13 regula hacia abajo la desmogleína-1 y la filagrina. La permeabilidad epitelial altereda puede conducir a un entorno permisivo que mejora la presentación de antígenos, lo que a su vez conduce al reclutamiento de eosinófilos.
Actividad Th2 aumentada y susceptibilidad alérgica
Varias líneas de evidencia apoyan el concepto de que la EE es una entidad mediada por la actividad de las células T helper 2 (Th2), inducida principalmente por los antígenos de los alimentos. En repetidas ocasiones, las series de casos han informado que los pacientes con EE tienen hipersensibilidad ambiental y alimentaria, responden a la eliminación de la dieta de los antígenos alimentarios y tienen una recaída cuando se reintroducen antígenos alimentarios similares.
Si bien los antígenos de los alimentos han sido identificados como los principalmente antígenos desencadenantes, los aeroalergenos inhalados también tienen su papel en algunos pacientes; este hallazgo puede representar la manifestación de la sensibilización cruzada a los alérgenos de los alimentos.
De hecho, en los modelos murinos de EE se puede hacer la sensibilización provocando a los ratones con aeroalergenos y albúmina de huevo, o por la sobreexpresión de citocinas presentes en los animales y que se hallan en la EE humana. Varias líneas de evidencia sugieren que la interleucina-5 y la interleucina-13 pueden representar un papel en la patogénesis de la EE.
En los modelos inducidos por alérgenos y en comparación con los ratones de tipo salvaje, los ratones interleucina-5 nulos desarrollan menos EE. En las muestras de biopsia de pacientes con EE se constata la sobreexpresión de interleucina-13, y se ha comprobado que la misma regula un número de citocinas relacionadas, tanto en estudios in vitro como en estudios en ratones.
Por otra parte, otros ensayos prospectivos han demostrado que el tratamiento con anticuerpos anti interleucina 5 o 13 reduce el número de eosinófilos esofágicos en niños y adultos. En los pacientes con EE también se halla una proliferación dirigida por citocinas y la linfopoyetina estromal tímica, reclutamiento de eosinófilos, mastocitos portadores de IgE, linfocitos Th2, basófilos y células killer naturales.
El mecanismo predominante de la alergia a los alimentos en la EEE parece ser un proceso no mediado por la IgE, porque el omalizumab, un tratamiento biológico anti IgE no es eficaz en los seres humanos, la eosinofilia esofágica puede desarrollarse en los ratones IgE nulos y células B nulos mientras que los tests cutáneos no identifican a los alérgenos alimentarios desencadenantes. Recientemente se ha demostrado que en el epitelio esofágico de los pacientes con EE está presente la IgG4 específica de los alimentos y reacciona a los 4 antígenos alimentarios desencadenantes más comunes.
Disfunción esofágica y potencial fibrótico
La esofagografía con contraste suele revelar un calibre esofágico reducido y menor distensibilidad
Puede ser de utilidad el uso de un dispositivo con balón intraluminal que mide la distensibilidad de la pared y que se utiliza para evaluar las estrecheces esofágicas y la fibrosis. Es útil incluso cuando la estrechez y la fibrosis no son detectables endoscópicamente.
Los primeros estudios con este dispositivo mostraron que los pacientes con una meseta de distensibilidad específica tenían menos probabilidad de haber sufrido impactación de alimentos, o de sufrir la impactación de alimentos durante el seguimiento.
La esofagografía con contraste en los pacientes con una complacencia parietal esofágica anormal suele revelar un calibre esofágico reducido y menor distensibilidad. La exposición in vitro de fibroblastos y células musculares lisas esofágicas al factor de crecimiento transformador β (TGF-β) conduce la contracción del músculo liso y la fibrosis.
Características clínicas
Epidemiología
Desde el establecimiento de pautas de diagnóstico y un código de diagnóstico (Clasificación Internacional de las Enfermedades, 9ª Revisión, código K20.), algunos estudios han estimado una prevalencia de la EE entre 1 y 5/10.000 personas en los Estados Unidos y Europa, y una prevalencia creciente en Asia. Ciertas subpoblaciones, como los pacientes que se someten a una endoscopia por antecedentes de impactación de alimentos, tienen una prevalencia significativamente mayor, de hasta 54%.
La EE ha sido descrita en todos los grupos de edad pero afecta predominantemente a los hombres de raza blanca, y pude comenzar desde la edad escolar hasta la edad media de la vida. Es común una historia personal o familiar de enfermedades atópicas, como asma, el eczema, rinitis y alergia anafiláctica a los alimentos; estas condiciones requieren tratamiento.
Presentación clínica
Los niños pueden tener una amplia variedad de síntomas inespecíficos, como dificultad para alimentarse, náuseas y vómitos, ardor de estómago y retardo del crecimiento. En contraste, los adolescentes y los adultos son más propensos a presentar disfagia y episodios de impactación de alimentos. Sin embargo, los grupos de pacientes de diferentes edades pueden tener síntomas en común-por ej., síntomas de reflujo crónico.
Los síntomas pueden ser subestimados por su larga data y acostumbramiento sutil, como comer despacio, masticar con cuidado, cortar los alimentos en trozos pequeños, comer alimentos con salsas, beber líquidos para diluir los alimentos y píldoras, y evitar los alimentos que puedan causar disfagia, como carnes y panes. Los pacientes pueden tener temor de comer en lugares públicos, por su preocupación de mostrar dificultades para comer.
En casos raros, la EE puede manifestarse con ruptura espontánea del esófago secundaria a arcadas forzadas (síndrome de Boerhaave) después de una impactación de alimentos. En el 30% de los pacientes adultos se produce ardor de estómago, especialmente con la ingestión de alcohol.
No está claro si antes de la presentación hubo años de enfermedad subclínica no reconocida en la infancia o de presentación "silenciosa" de la inflamación crónica en los adultos, o si los pacientes adultos verdaderamente tienen un inicio tardío de la enfermedad o una patogénesis o fenotipo diferentes de la enfermedad.
En apoyo a la hipótesis que la enfermedad subclínica no reconocida en la infancia o la inflamación crónica silenciosa preceden a la presentación surge de un estudio de la evolución natural en el que se observó que el 85% de los adultos con síntomas no tratados durante 20 años desarrollaron estrecheces esofágicas.
Imágenes de la esofagitis eosinofílica
La endoscopia y la radiografía contrastada son herramientas complementarias para evaluar la EE. Los hallazgos endoscópicos más comunes son manchas blancas (que representan exudados eosinófilos), edema mucoso, surcos lineales, anillos esofágicos, y remodelación crónica de las estrecheces, representadas por las estenosis; en el denominado "esófago papel crepé", los surcos lineales se producen en respuesta a un trauma mínimo, como puede ser el paso del endoscopio. También se produce el "signo del tirón," una sensación firme detectada por el endoscopista al realizar una biopsia esofágica.
Recientemente se ha validado un sistema de puntos para los hallazgos endoscópicos, con el fin de estandarizar la evaluación de los signos de la EE, como la presencia de edema, anillos, exudados, surcos y estenosis (EREFS).
El reconocimiento de la EE como una entidad diagnóstica ha conducido a un mayor uso de la esofagografía con bario para evaluar la luz del esófago en los pacientes con disfagia. A diferencia de las estenosis esofágicas distales focales halladas en los pacientes con ERGE, la estenosis de los pacientes con EE puede ser larga y cónica y comúnmente escapa a la detección endoscópica, pero son evidentes en el esfigmograma con contraste.
Dos estudios recientes informaron que el 71% de los adultos y el 55% de los niños con EE no tenían estrechez esofágica reconocida en la endoscopia pero tampoco se hallaron en el esófagograma.
Características histológicas de la esofagitis eosinofílica
La EE se caracteriza por un aumento del número de eosinófilos en el epitelio del esófago, el cual típicamente carece de esas células. Se cree que el uso de un valor de corte de al menos 15 eosinófilos por campo de gran aumento brinda una sensibilidad del 100% y una especificidad del 96% para establece el diagnóstico histológico de EE, aunque se han descrito pacientes con menores niveles de eosinofilia y características fenotípicas de la EE.
Es típica pero no patognomónica la presencia de agregados y capas de eosinófilos, o de microabscesos a lo largo de la superficie luminal. Otros patrones de lesión asociados son los espacios intercelulares dilatados, la elongación de las crestas interepiteliales y la hiperplasia de las células basales. En el espacio epitelial afectado también hay un aumento de las células inflamatorias, incluyendo linfocitos, mastocitos y basófilos.
| La tinción de rutina con hematoxilina y eosina revela numerosos eosinófilos (flechas finas), espacios intercelulares dilatados (flechas gruesas), hiperplasia de la zona basal (círculos) y elongación papilar (soporte). |
Complicaciones y Condiciones asociadas
Las complicaciones que pueden ocurrir en asociación con la EE son la estenosis esofágica, la impactación de alimentos, la perforación del esófago y la desnutrición, no así el cáncer. También se han hallado otras asociaciones como la enfermedad del tejido conectivo, la enfermedad celíaca y la enfermedad de Crohn.
Tratamiento
Identificación de los puntos finales de los tratamientos validados
Los pacientes con EE pueden tener un desfasaje entre los síntomas y las características histopatológicas, lo que crea la necesidad de realizar múltiples evaluaciones de la actividad de la enfermedad.
Como resultado, los objetivos terapéuticos a corto plazo son el alivio de los síntomas, el control de la inflamación y la restauración funcional. Para alcanzar estos objetivos se pueden utilizar 3 enfoques terapéuticos: dietoterapia, medicamentos y dilatación esofágica. Siempre que sea posible, el tratamiento debería estar dirigido por un equipo médico que incluya un gastroenterólogo, un alergista y un nutricionista.
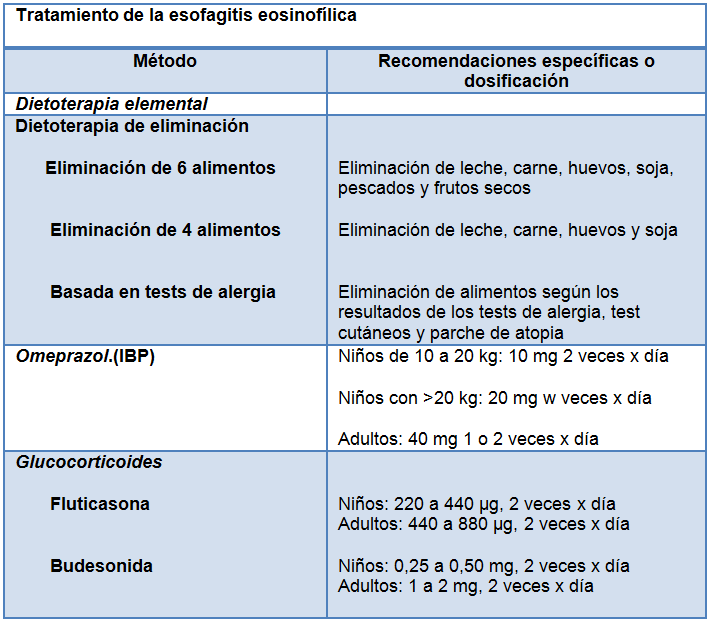
Dieta
En 1995, un estudio de 10 niños con EE describió los efectos favorables de una dieta basada exclusivamente en aminoácidos (es decir, carente de antígenos de los alimentos). Tanto los síntomas como las alteraciones histológicas mejoraron pero reaparecieron después de la reanudación de la dieta normal. Este pequeño estudio fue seguido por un estudio mucho más grande y otro estudio similar con la participación de adultos.
En estos estudios, los pacientes respondieron casi por completo al tratamiento, y el escenario estaba listo para el uso rutinario de la dietoterapia destinada a la EE. Sin embargo, los costos y la falta de interés de los pacientes en una dieta elemental condujeron al desarrollo de otras 2 estrategias de dieta. Se ha demostrado que el uso del parche atópico por punción cutánea o el test de la IgE sérica específica realizado por un alergólogo para determinar las dietas específicas tienen un alto grado de éxito en los niños.
Sin embargo, un trabajo más reciente Indica que este enfoque puede no ser tan efectivo como se pensaba al principio, ya que solo el 45% de los pacientes tiene una respuesta sostenida. No obstante, las dietas de eliminación y la evitación de la anafilaxia alimentaria, a cargo de un alergista, son opciones terapéuticas razonables.
Una dieta alternativa propuesta no está basada en pruebas de alergia alimentaria sino que elimina los 6 tipos de alimentos alergénicos más comúnmente identificados (trigo, leche, soja, frutos secos, huevos y mariscos). Esta dieta, denominada de eliminación de 6 alimentos, mejoró los síntomas y las anormalidades histológicas hasta en 26 de los 35 niños y 32 de los 50 adultos dentro de las 6 semanas. Los estudios de seguimiento están evaluando enfoques menos rigurosos en el que inicialmente se eliminan menos alimentos.
La dietoterapia puede ser muy eficaz y abordar directamente el mecanismo alérgico subyacente. También se puede lograr el objetivo de Identificar el número limitado de antígenos de los alimentos que desencadena la respuesta inflamatoria.
Por ejemplo, debido a que la endoscopia con biopsia es actualmente el único método confiable para evaluar la respuesta histológica, cada paciente puede tener que someterse a múltiples exámenes para identificar los alimentos que desencadenan la EE.
Actualmente se está evaluando una prueba menos invasiva, consistente en una esponja deglutida, que se realiza sin anestesia, a la noche, a la cabecera del paciente. La preocupación que despierta la dietoterapia se debe al mayor costo de los alimentos, la mala adherencia a la dieta y las deficiencias nutricionales secundarias a la eliminación de los alimentos.
Fármacos
Inhibidores de la Bomba de protones
Estos fármacos pueden representar un papel en la evaluación diagnóstica de los pacientes con sospecha de EE y en el cuidado de aquellos que padecen la enfermedad.
- Primero: el único criterio disponible en la actualidad para descartar la ERGE como causa de la EE es la falta de respuesta a los IBP.
- Segundo: los pacientes con EE confirmada también pueden tener ERGE sintomática que responde a los IBP y contribuye al desarrollo de EE.
Tercero: los estudios in vitro muestran que los IBP disminuyen la secreción de citocinas en el epitelio esofágico, independientemente de su efecto sobre la secreción de ácido, lo que lleva a la hipótesis de que los IBP pueden proporcionar un beneficio antiinflamatorio. Estos estudios in vitro definen más un subgrupo de pacientes con un fenotipo de EE, en la que la eosinofilia esofágica responde a los IBP, un fenómeno denominado EE sensible a los IBP.
Estudios posteriores de pacientes con EE sensible a los IBP demostraron que la las características clínicas, histológicas y genéticas son similares a las de los pacientes con EE, lo que apoya la posibilidad de que la condición sea un subtipo de EE. Sin embargo, la diferente respuesta a los IBP en el caso de la condición provocada por los alérgenos alimentarios puede diferenciar la EE sensible a los IBP de la EE.
Glucocorticoides tópicos
La fluticasona por vía oral o en aerosol o una preparación de budesonida líquida viscosa son los pilares de la terapia farmacológica
Los glucocorticoides actúan sobre los mecanismos clave de la EE. Por ejemplo, disminuyen la fibrosis por reducción de las células inflamatorias. Por otra parte, el aumento de los niveles del ARNm de la interleucina-13 (un regulador central de las enfermedades alérgicas) y el transcriptoma de la EE son en gran parte reversibles con el tratamiento glucocorticoide in vivo.
Aunque no han sido aprobadas por la Food and Drug Administration, la fluticasona por vía oral o en aerosol (mediante un inhalador con medidor de dosis) o, una preparación de budesonida líquida viscosa son los pilares de la terapia farmacológica para la EE.
La eficacia de estos medicamentos tópicos para mejorar los síntomas y las anomalías histológicas después de 2 a 12 semanas de aplicación oscila entre el 53% y el 95%. Los glucocorticoides tópicos también pueden reducir la frecuencia de las posteriores impactaciones de alimentos.
Un estudio ha apoyado la observación de que la budesonida oral viscosa tiene un contacto más prolongado con la mucosa esofágica y cubre una mayor longitud del esófago que la budesonida nebulizada. Los análisis genómicos recientes pueden ayudar a identificar si los pacientes que serán más o menos propensos a tener una respuesta al tratamiento con glucocorticoides.
Los efectos secundarios posibles son la infección local por cándida, la supresión del eje suprarrenal, la desmineralización ósea y el retardo del crecimiento. Debido a que los glucocorticoides tópicos ingeridos se someten al primer paso metabólico, dichos efectos a parecen ser poco frecuentes. Sin embargo, el uso de glucocorticoides sistémicos provoca resultados terapéuticos similares y mayor riesgo de efectos secundarios que su uso tópico.
Dilatación
La dilatación esofágica destinada a aliviar la estenosis del esófago es una terapia comúnmente aceptada para la EE, en particular en los adolescentes y los adultos mayores. Mientras que los informes anteriores mostraban una tasa elevada de complicaciones relacionadas con la dilatación, una revisión de grandes series de casos mostró que la tasa de perforación es inferior al 1% (3 de 992 dilataciones).
En los pacientes con EE, la dilatación debería ser realizada gradualmente en varias sesiones, con la expectativa de que el 75% de los pacientes tendrá dolor en el pecho después del procedimiento (una evolución que difierre de la de los pacientes con ERGE). La dilatación aborda con éxito la estenosis luminal que complica a la EE pero no trata el proceso inflamatorio subyacente.
Complicaciones a largo plazo, calidad de vida y tratamiento de mantenimiento
Una de las cuestiones controvertidas en el manejo de la EE es el papel del tratamiento de mantenimiento a largo plazo. La evidencia hasta la fecha Indica que la enfermedad no es premaligna y no acorta la vida. Por otra parte, los períodos prolongados de remisión, espontáneos o inducidos por la dilatación, pueden presentarse sin necesidad de hacer cambios en la dietoterrapia.
Sin embargo, en la mayoría de los pacientes, la EE es una enfermedad crónica, y si el tratamiento se interrumpe, la inflamación y los síntomas reaparecen, con disminución de la calidad de vida y la vitalidad, reduciendo posteriormente los puntajes generales de salud, con complicaciones tales como la estenosis.
Pocos estudios han examinado el beneficio a largo plazo de la dieta o el tratamiento tópico con glucocorticoides, aunque ambos han sido las opciones que se han propuesto para el tratamiento de mantenimiento en la remisión.
Según el consenso de expertos, hay evidencia de que la ausencia de tratamiento conduce a la remodelación crónica y la aparición de estenosis largas o esófago de pequeño calibre, historia de impactaciones alimentarias o síntomas graves, como así la rápida recurrencia de la enfermedad, lo que indica la necesidad de tratamiento de mantenimiento.
Conclusiones
Desde la descripción inicial de la EE en series de casos hace más de 20 años, el interés al respecto ha ido creciendo, y ahora hay una mayor conciencia de las características clínicas, mecanismos básicos y opciones terapéuticas eficaces.
El advenimiento de las caracterizaciones moleculares y diagnósticas dará lugar a la determinación de nuevas estrategias terapéuticas.
El tratamiento de la EE requerirá de una mayor comprensión de las implicancias de esta enfermedad crónica de probable duración para toda la vida, el desarrollo de nuevos enfoques terapéuticos y la documentación de la seguridad y eficacia de las terapias a largo plazo.





